一、電子殼層與能階:
- 想象電子分布在以原子核為中心的球體上,從內向外為K層、L層及M層,電子存在的殼層稱為電子殼層。
- 電子(帶負電)處於:
越靠近原子核(帶正電)的殼層,被原子核束縛越大,能量越低,越安定;
電子處於越遠離原子核越遠的殼層,能量越高,越不安定。電子殼層 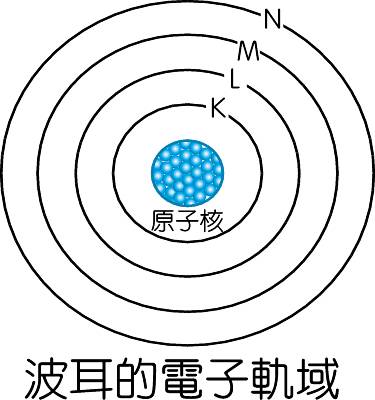
- 電子能量由距離原子核近至遠,呈現階梯式的遞增,稱為能階。
- 若依拉塞福的行星原子模型,電子繞核運轉將消耗的能量使電子繞轉轉半徑愈來愈小,最後撞入原子核而消滅,而所放出的光譜也應是連續光譜,因此拉塞福的行星原子模型並無法解釋實際的情形。
- 波耳提出了氫原子的原子模型,保留部份拉塞福的行星原子模型加入能量量子化以及物質波的概念。
- 波耳認為:
- 電子只待在特定的軌道上運動,並將軌道由小到大用n=1、2、3、...編號。
- 電子在不同軌道上具有不同的能量,用En=-2.179×10-18/n2 焦耳來代表第n個軌道上的能量。(僅適用於單電子原子,如H、He+)
- 電子可由外界吸收能量而由低階躍升至高階,所吸收之能量相當於兩能階之能量差,即△E=EH-EL;
反之,電子由高階降至低階,則會釋放出能量。此能量常以光的形式被吸收或放出。電子由高階降至低階,則會釋放出以光的能量形式被放出。 電子由高階降至低階,則會釋放出以光的能量形式被吸收。
-
電子從低能階躍遷到高能階,需吸收能量;
電子從高能階躍遷到低能階,需放出能量。 -
電子填入電子殼層的原則:
-
每一殼層最多可容納的電子個數不同,越外層的殼層離原子核越遠,範圍越大,可容納的電子數越多。
殼層 n 可容納電子數(2n2) K 1 2 L 2 8 M 3 18 N 4 32 - 電子依序從最接近原子核能量最低的殼層,開始填起。待填滿後再依序填入離原子較遠,且能量較高的殼層。
-
每一殼層最多可容納的電子個數不同,越外層的殼層離原子核越遠,範圍越大,可容納的電子數越多。
- 原子中佔據最外殼層的電子稱為價電子,價電子所分布的殼層稱為價殼層。
- 原子的性質主要繫於價電子。因為價電子距離原子核最遠,受原子核的束縛最小,因此在化學反應中最容易發生移轉,故價電子所在價殼層的個數與該元素的化學性質有關;同一族元素有相似的價殼層(氫除外),故同族元素有相似的化學性質。



