一、結構式定義
原子間以短線(化學鍵)相連,表示分子內原子和原子間,鍵結情形的化學式。稱為結構式。
| 元素族數 | 6A | 5A | 4A |
|---|---|---|---|
| 鍵結量 | 2 | 3 | 4 |
| 例如 | H2O | NH3 | CH4 |
| 結構式 | H-O-H | 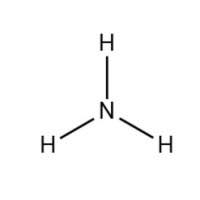 | 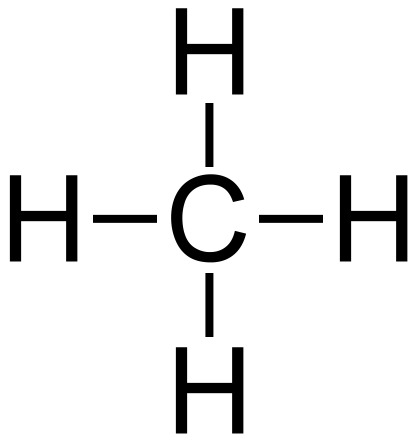 |
| 球-棍模型 | 缺 | 缺 | 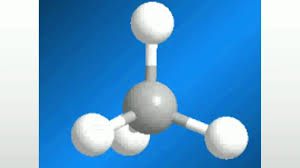 |
| 空間填充模型 | 缺 | 缺 | 缺 |
二、結構式的特性。
- 結構式中連結原子間的短線稱為化學鍵。
- 不同的元素有不同的鍵結量,依各元素的鍵結量將分子畫出的模型是球-棍模型和空間填充模型等分子模型。可更準確表示分子於三度空間中的相對位置。
- 同分異構物:分子式相同,而結構式不同的化合物。稱為同分異構物。
因原子間的排列方式,決定分子的性質,所以其物理性質、化學性質亦不相同。
| 名稱 | 乙醇 | 甲醚 |
|---|---|---|
| 分子式 | C2H6O | C2H6O |
| 結構式 | 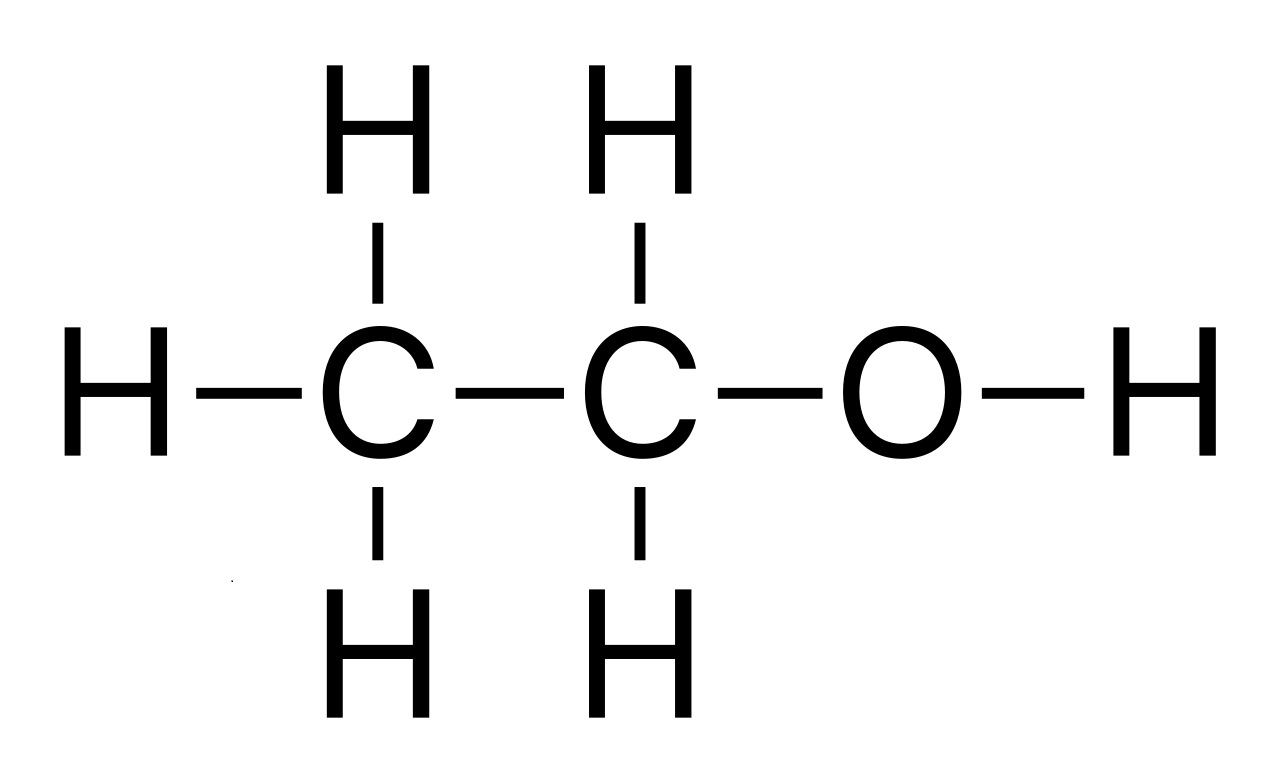 | 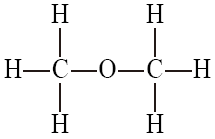 |
| 球-棍模型 | ||
| 熔點 | -114.5 | -138.5 |
| 沸點 | 78.4 | -23 |
三、結構式的限制。
結構式並非分子真正的形狀。真正的形狀需以分子模型才能表示。
四、式性式。
有機化合物性質會受某些特定原子團的影響,這些原子團稱為官能基。有機分子內含有某種官能基,可表示其特性的化學式稱為式性式。常採用在有機化合物中。

