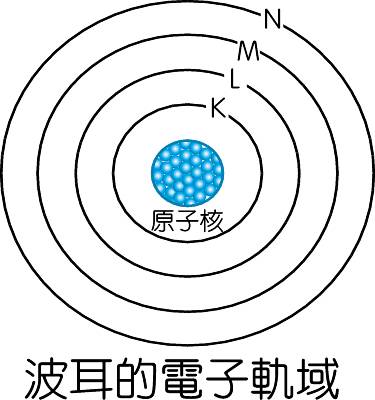
一、原子的組成:
原子是由原子核和核外電子所形成,其中原子核包含質子和中子。
| 原子 | 電子(1897湯木生發現) | 電量(帶負電):-1.602×10-19庫倫。質量為質子的1/1836倍。 | |
| 原子核(1911拉塞福發現) | 質子(1919拉塞福發現) | 電量(帶正電):與電子等值異號。 | |
| 中子(1932查兌克發現) | 電量(不帶電):質量約與質子相當。 | ||
二、元素符號:
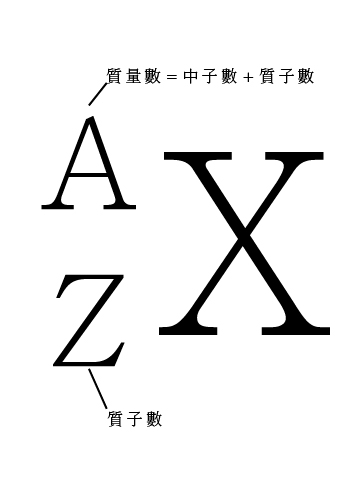
三、同位素:
- 定義:相同原子序,質量數不同的原子。
- 同位素之間物理性質不同,化學性質相似,故無法以化學方法分離。
- 比較:
- 相異點:中子數、質量數、物理性質。
- 相同點:化學性質、電子數、質子數(原子序)。
| 元素 | 氫 | ||
| 同位素 | 氫(H) | 氘(D) | 氚(T) |
| 名稱 | 氫-1 | 氫-2 | 氫-3 |
| 電子數 | 1 | ||
| 質子數 | 1 | ||
| 中子數 | 0 | 1 | 2 |
| 自然界含量(%) | 99 | 0.015 | 極微量 |