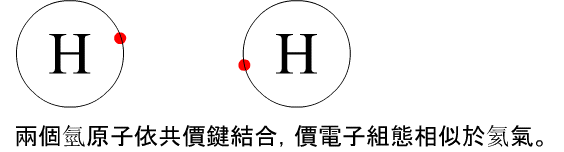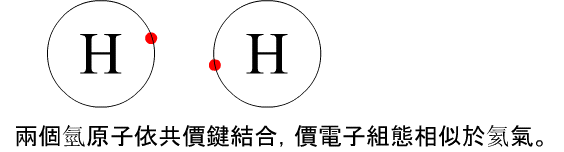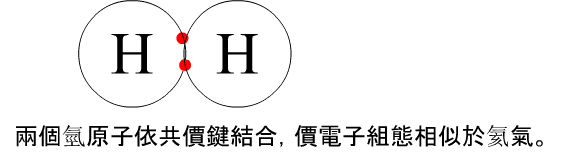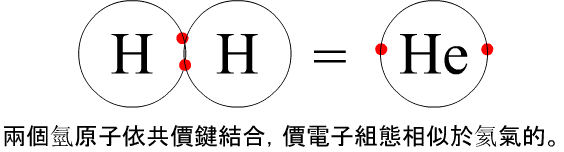
一、路易斯電子點式:
- 提出者:美國化學家路易斯。
- 內容:鈍氣在室溫下均為單原子氣體。除了氦只有2個價電子,其它均有8個價電子,且不易和其他原子反應,具有特殊的穩定性,故鈍氣的穩定性與其價殼層,完全填滿有關。
- 八隅體規則:穩定化學鍵的形成是藉由原子間的價電子轉移或共用,使各原子的電子都排列到如同鈍氣的電子組態。

二、化學鍵:
- 定義:原子間可藉由得、失或是共用價電子的方式來滿足八隅體規則,以形成各種物質,此時原子間互相結合的作用力、吸引力就稱為化學鍵。
- 種類:可區分為離子鍵、共價鍵和金屬鍵。
註:路易斯結構
路易斯結構(英語:Lewis structures),又稱路易斯點圖像、電子點圖像、路易斯電子點式、路易斯點結構、電子點結構,是分子中原子和原子鍵結和標示孤對電子存在的圖像。路易斯結構可以畫出表示分子中的共價鍵以及配位化合物。
路易斯結構是以美國物理化學家吉爾伯特·路易斯(Gilbert Newton Lewis)的名字命名,他在1916年時把路易斯結構寫入它的一篇名為《原子和分子》的文章中。
它們類似電子點圖像在價電子和孤對電子中以點來表示,但也可以用線來表示共享電子(如單鍵、雙鍵、三鍵等)。
路易斯結構中每個原子他們的位置在分子的結構上用不同的化學記號標示。
線畫在原子和原子間的鍵結(也可以用一對點來表示),多餘的電子以一對點來表示孤對電子。
雖然第二週期的主族元素可反應藉由獲得或失去共享電子讓外層價電子填滿至8個,然而其他元素對於價電子遵循不同的規則。
例如:氫原子(H)的遵循方式是填滿最外層的一個價電子或使之最外層沒有電子。
註:路易斯電子點式規則步驟:
-
計算總價電子數
- 計算分子中所有原子的總價電子數。
-
如果是陰離子,則需加上電子的數量;
如果是陽離子,則需減去電子的數量。
-
排列原子
- 選出中心原子,通常是分子中電負度最小的原子(氫除外)。
- 將其他原子排列在中心原子周圍。
-
畫出鍵結
- 在原子之間畫單鍵(一對點)來表示共價鍵。
- 如果多個原子之間是雙鍵或三鍵,則用兩對或三對點表示。
-
填入孤對電子
- 從總價電子數中減去用於鍵結的電子,剩下的電子以孤對電子(兩點)的形式填入原子周圍。
- 優先填入外層原子,直到每個原子都滿足八隅體規則(氫原子為兩點)。
- 如果還有剩餘的電子,則填入中心原子。
-
調整鍵結
- 如果有些原子尚未滿足八隅體規則,則將中心原子的孤對電子移動,與其他原子形成多重鍵(雙鍵、三鍵等),直到所有原子都滿足八隅體規則。
-
標示離子
- 如果是離子,則在整個結構外加上括號,並將其電荷寫在括號的右上方。