化學
-
第24題,答案:D
下列關於原子能階的敘述,何者錯誤?
(A)原子中的電子可能處在不同的能階(○)
(B)一個氫原子雖然只有一個電子, 但能階躍遷時可能發射不同波長的光子(○)
(C)原子中的電子吸收能量後, 可能從較低的能階躍遷到較高的能階(○)
(D)為了使處於穩定狀態之原子的電子維持在特定的能階上,外界必須持續提供特定能量的光子(✖)
<修正>為了使處於穩定狀態之原子的電子維持在特定的能階上,外界無須持續提供能量。
(E)原子中的電子從一個能階躍遷到另一個能量較低的能階時, 會放出光子(○)
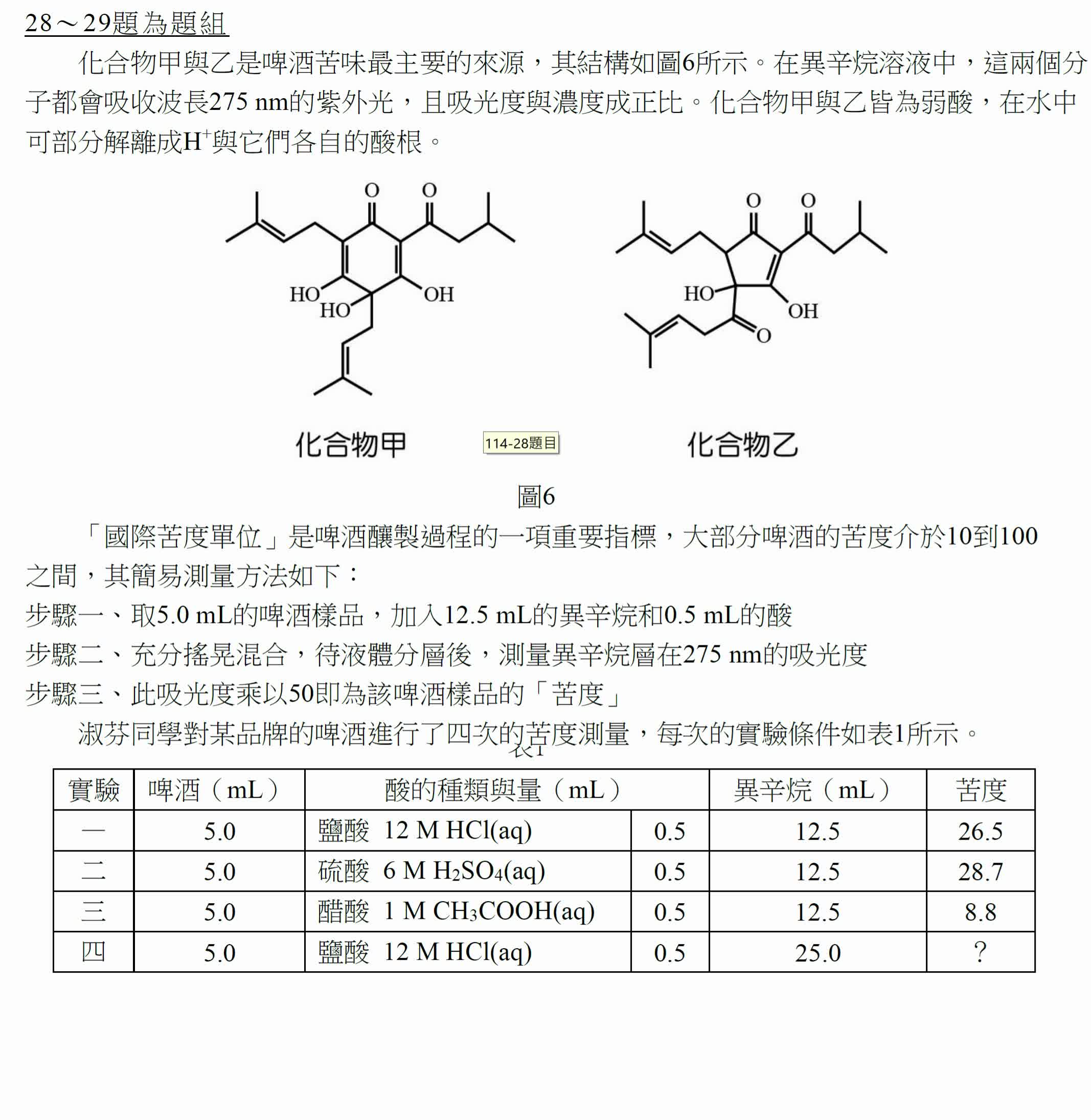
第28題,答案:A、C
下列相關的敘述,哪些正確?(應選2項)
(A)化合物甲的分子式為C21H30O5
(B)化合物甲與乙皆具有20個碳原子
<修正>有21個碳原子。
(C)化合物甲與化合物乙互為異構物
(D)苦度與化合物甲與乙的總濃度成反比
<修正>正比
(E)加入異辛烷的目的是為了使啤酒與實驗所添加的酸能夠更均勻混合
<修正>加入異辛烷的目的是為了萃取啤酒中的化合物甲乙。
第29題,答案:A、E
下列關於實驗的敘述,哪些正確?(應選2項)
(A)實驗三的苦度值與實驗一、二差異大,說明實驗所使用的酸的強弱會影響苦度值的測量
(B)實驗四中的苦度數值約為53
<修正>實驗四中的苦度數值約為13。
(C)若在實驗一中,不加入鹽酸,改為加入0.5 mL的12 M NaOH(aq),則水溶液中酸根的濃度會下降
<修正>若在實驗一中,不加入鹽酸,改為加入12 M的NaOH(aq) 0.5 mL,則有益於發生酸鹼反應,造成水溶液中酸根的濃度會上升。
(D)若在測量方法使用10.0 mL的啤酒樣品,其他步驟不變,則量測的苦度值會變低
<修正>若在測量方法使用10.0 mL的啤酒樣品,其他步驟不變,啤酒量增加,化合物甲乙也增加,則量測的苦度值會增加。
(E)步驟二使用到萃取法
-
第30題,答案:A、C
關於物質純化與分離的敘述,下列哪些正確?(應選2項)
(A)利用再結晶純化硝酸鉀,以水為溶劑會比汽油較為合適
(B)硫酸鈉晶體可由飽和的藍色硫酸銅水溶液中結晶獲得
<修正>飽和的藍色硫酸銅水溶液中無硫酸鈉故無法結晶獲得硫酸鈉晶體。
(C)將食鹽水加熱,蒸餾出部分純水,而剩餘的溶液可再結晶獲得氯化鈉
(D)利用乙酸乙酯萃取綠色樹葉的萃取液,然後在一大氣壓下進行蒸餾分離,可以將葉綠素餾出
<修正>利用乙酸乙酯萃取綠色樹葉的萃取液,然後在一大氣壓下進行蒸餾分離,可以將沸點低的乙酸乙酯餾出。
(E)硝酸鉀與氯化鉀的混合水溶液,可以用濾紙層析方法將兩者分離
<修正>硝酸鉀與氯化鉀的混合水溶液,無法用濾紙層析方法將兩者分離。
-
第31題,答案:B、D、E
乙酸和乙醇在硫酸催化下,可進行酯化反應如式1,假設乙酸與乙醇皆反應完全無殘留,蒸餾後可製得乙酸乙酯。氯化氫和氫氧化鈉的水溶液可進行反應如式2,與酯化反應類似,可產生一分子的水。
CH3COOH(aq) + C2H5OH ⎯⎯(硫酸、加熱)⎯→ CH3COOC2H5(l) + H2O(l)... 式1
HCl(aq) + NaOH(aq) ⎯⎯(室溫)⎯→ NaCl(aq) + H2O(l)... 式2
比較這二類反應,試問下列敘述,哪些正確?(應選3 項)
(A)式1與式2 的反應皆可寫成淨離子反應式:H+(aq) + OH-(aq) → H2O(l)
<修正>只有式2 的反應可寫成淨離子反應式:H+(aq) + OH-(aq) → H2O(l)。
(B)乙酸與氯化氫溶於水,可解離出H+,兩者皆為電解質
(C)乙酸與氯化氫溶於水,可解離出H+,兩者皆為離子化合物
<修正>乙酸與氯化氫皆是共價鍵結合的 分子化合物。
(D)利用蒸餾法可取得乙酸乙酯,是利用產物間沸點不同的性質做分離
(E)式2 為放熱反應
-
第32題,答案:C
萊克多巴胺俗稱「瘦肉精」,可作為動物飼料添加物,用以幫助肌肉生長,減少體脂肪。將「瘦肉精」樣品進行元素分析,發現含有重量百分比71.75 %的碳、7.65 %的氫、4.65 % 的氮與15.95 %的氧,試問其分子式為何?(原子量:H=1.0,C=12.0,N=14.0,O=16.0)
(A)C18H25N2O2(✖)
(B)C17H22N2O2(✖)
(C)C18H23NO3(○)
(D)C17H21NO4(✖)
(E)C17H21N2O3(✖)
<修正>元素分析求最簡整數比:C:H:N:O = (71.75/12):(7.65/1):(4.65/14):(15.95/16) = 6:7.65:0.33:1 → 乘3 得 18:23:1:3,所以分子式為 C18H23NO3。
-
第33題,答案:A、E
關於聚合物的敘述,下列哪些正確?(應選2項)
(A)纖維素與澱粉都是以葡萄糖為單體的聚合物(○)
(B)蛋白質是以核苷酸為單體的聚合物(✖)
<修正>蛋白質是以胺基酸為單體的聚合物。
(C)DNA是以葡萄糖與胺基酸為單體交錯形成的聚合物(✖)
<修正>DNA是以核苷酸為單體形成的聚合物。
(D)脂肪是以脂肪酸為單體的聚合物(✖)
<修正>脂肪不是聚合物;主要由甘油+脂肪酸酯化形成。
(E)RNA是以核苷酸為單體的聚合物(○)
-
第34題,答案:E
圖7是三種氣體於不同溫度下在水中的溶解度。此外,小華上網查了CO2於0 ℃、20 ℃、40 ℃與60 ℃在水中的溶解度,分別是0.334、0.169、0.097、0.058(單位:g/100g水)。下列相關的敘述,何者正確?
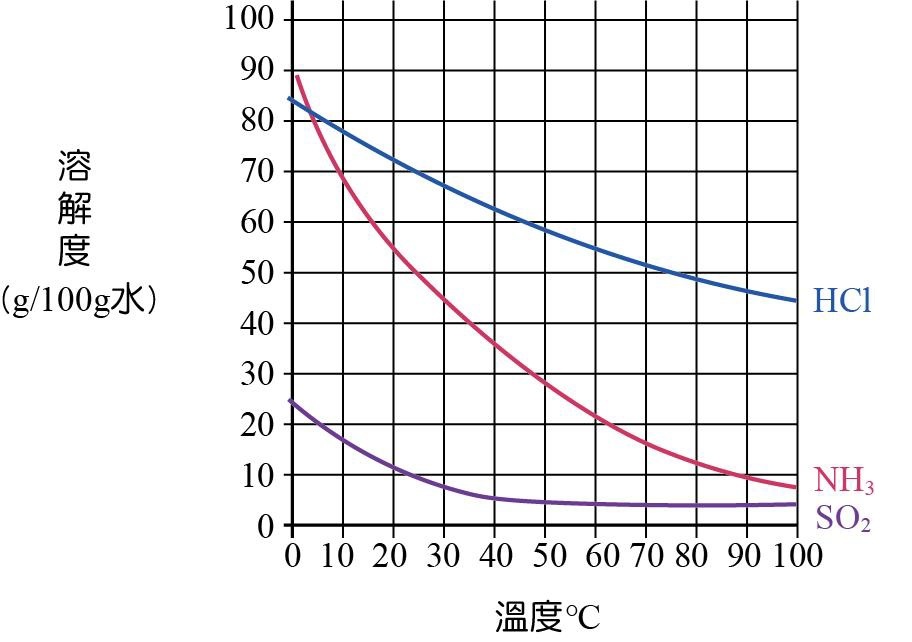
(甲) 在0°C時,氨氣在水中的溶解度大小順序為NH3<HCl<SO2(✖)
<修正>在0°C時,溶解度大小順序為 SO2<HCl<NH3。
(乙) 在0~60°C之間,溫度升高時,氨氣在水中的溶解度降低(○)
(丙) 將4°C含CO2氣泡飲料置於大熱時,會產生打開瓶蓋時二氧化碳噴出的影響(○)
(丁) 氣體溶解度的變化主要受溫度變化的影響(○)
(A)只有甲(✖)
(B)只有乙(✖)
(C)只有丙(✖)
(D)甲與乙(✖)
(E)乙與丙(○)
-
35~36 題為題組:
氧化亞銅為一種半導體材料,其奈米粒子會懸浮在水中,表面可以吸收光能,將二氧化碳轉化成甲醇(CH3OH)與氧氣,但氧化亞銅奈米粒子並不會被消耗。持續通入二氧化碳於含氧化亞銅的水溶液中使反應進行,發現光照期間,可觀察到氧氣生成;若將光源關閉,則沒有氧氣生成。 第35題,答案:A、C、E
35.關於實驗結果與推論的敘述,下列哪些正確?(應選3項)
(A)二氧化碳進行還原作用產生甲醇
(B)含有二氧化碳的水溶液呈鹼性
<修正>二氧化碳溶於水形成碳酸故含有二氧化碳的水溶液呈酸性。 (C)光照是產生甲醇的必要條件
(D)此反應所產生的甲醇
與氧氣均難溶於水中
<修正>甲醇易溶於水 (E)此光照反應式為:2CO2 + 4H2O → 2CH3OH + 3O2(應選3項)
<修正>你提供的截圖中第35題 A~E 選項文字解析度不足,無法逐字照抄;若補一張清晰截圖,我可把每一個選項加上(○/✖)並用紅字逐句修正。
第36題,答案:C
經過更仔細的實驗觀察,發現另有少量為氫氣的副產物生成,可能是在光照下,水亦可被分解為氫氣與氧氣,反應式為:2H2O → 2H2 + O2。若某次實驗結果的氣體產物為氧氣1.40 莫耳與氫氣0.40 莫耳。試問該次實驗生成多少莫耳的甲醇??
(A)0.4(✖)
(B)0.6(✖)
(C)0.8(○)
(D)1.0(✖)
(E)1.2(✖)
<修正>由 2H2O → 2H2 + O2 得 H2:O2=2:1,0.4 mol H2 對應 0.2 mol O2(副產物)。
<修正>O2總量 1.40 mol,主反應產生 O2 為 1.40−0.20=1.20 mol。
<修正>由 2CO2 + 4H2O → 2CH3OH + 3O2 得 CH3OH:O2=2:3,故 CH3OH = 1.20×(2/3)=0.80 mol。
-
第50題,答案:B、E
奈米級的二氧化鈦(TiO2)為一種光觸媒材料,當此光觸媒照光之後,可將周遭環境中的汙染物質分解,達到去汙與除臭 的效果。而其原理主要是二氧化鈦光觸媒照光後,電子會從價帶躍遷到導電帶,使得二氧化鈦表面生成氫氧自由基(•OH)與超氧離子 (O2-),此兩者的活性很大可以將有機物分解成二氧化碳和水,達到淨化效果。 此外,二氧化鈦光觸媒亦可在光的照射下催化水裂解產生氫氣和氧氣,為綠色能源與永續發展的重要觸媒。由於二氧化鈦光觸媒的導電 帶與價帶的能階差(亦稱為能隙)大約為3.20 eV,故所照的光源中光子能量必須高於此能量才能啟動催化反應,為了提升其催化活性 與效率,許多研究利用不同的金屬摻雜來改善材料特性。某研究團隊發現於二氧化鈦奈米材料中摻雜少量的鋅離子 (Zn-TiO2)後,會改變能隙,並提升催化水裂解的效率。根據上述資訊及所學,回答下列問題。
下列與二氧化鈦的相關敘述,何者正確?(應選2項)
(A)提供電子能量必可使電子由價帶跳到導電帶(✖)
<修正>是須提供電子足夠的能量才可使電子由價帶跳到導電帶。
(B)電子位於導帶的能量比位於價帶低(○)
(C)可利用改變光的入射角來變化光子的能量(✖)
<修正>光子能量由 E=hc/λ 決定,與入射角無關。
(D)加大照光強度與面積可能促使無法躍遷的電子躍遷(✖)
<修正>無法藉由加大照光強度與面積促使無法躍遷的電子躍遷。
(E)增高照射的光頻率可能促使無法躍遷的電子躍遷(○)
-
第51題,答案:(a) 390 nm (b) Zn–TiO2

(a)...試計算波長約為多少nm?
<修正>3.2 eV = 3.2×1.6×10-19=5.12×10-19 J,且 E=hc/λ。
<修正>λ = (6.63×10-34×3.0×108)/(5.12×10-19) = 3.9×10-7 m = 390 nm。
(b)...兩樣本對400 nm的光激發產生的效應差異為何?
<修正>摻鋅後(Zn–TiO2)使材料可在 400 nm 光下發生激發反應,提升光觸媒效率。
-
第52題,答案:C、E
有關二氧化鈦光觸媒與水裂解反應的相關敘述,下列哪些正確?(應選2項)
(A)二氧化鈦光觸媒照光後產生的氫氧自由基具有8個價電子(✖)
<修正>氧氣自由基(如 O2•−)的價電子數判斷不應寫成「8個」 ;本敘述不正確;二氧化鈦光觸媒照光後產生的氫氧自由基具有7 個價電子。
(B)二氧化鈦是一種可溶於水的化合物(✖)
<修正>二氧化鈦為難溶於水的化合物。
(C)水裂解產生氫氣與氧氣,為一吸熱反應(○)
(D)氫氧自由基將有機物分解,產生二氧化碳的過程是作為還原劑(✖)
<修正>氧氣自由基通常扮演氧化劑,使有機物被氧化成CO2。
(E)水裂解反應產生氫氣與氧氣,屬於氧化還原反應(○)
-
第53題,答案:4倍
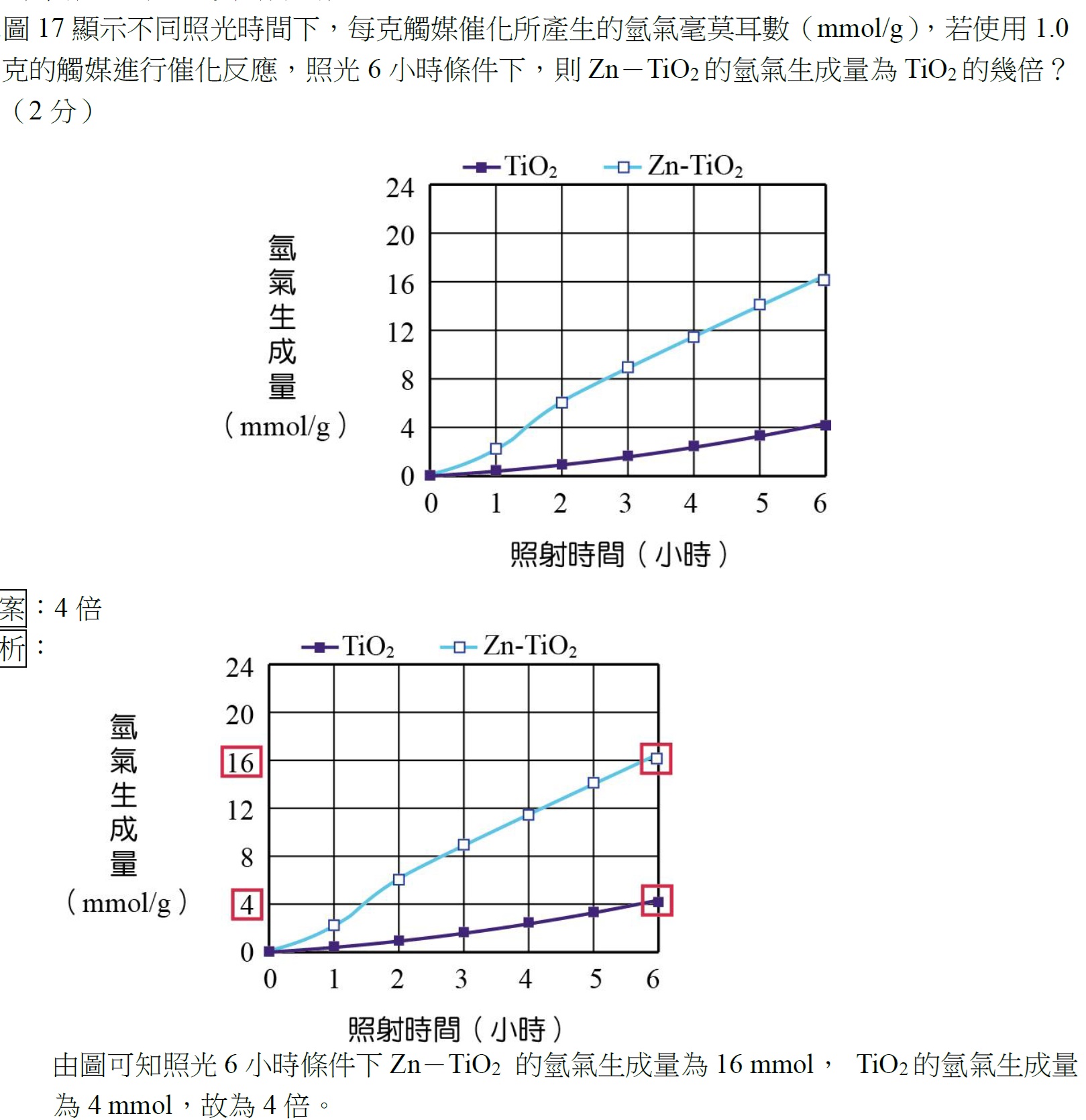
<修正>由圖可讀:6小時 Zn–TiO2 生成 16 mmol,TiO2 生成 4 mmol,比例為 16/4=4 倍。
-
第54題,答案:TiCl4 + 2H2O → TiO2 + 4HCl
二氧化鈦光觸媒可用不同的方法製備,其中之一是將四氯化鈦與水反應產生二氧化鈦,此反應亦會同時生成氯化氫。 試寫出此化學反應式(係數以最簡整數表示)。
<修正>配平後:TiCl4 + 2H2O → TiO2 + 4HCl。
-
第55題,答案:B
…根據表3資料,下列敘述何者正確?
(A)…1莫耳辛烷比1莫耳甲烷含有較多的分子數(✖)
<修正>同為 1 莫耳,分子數皆為阿伏加厥常數,不因分子量不同而改變。
(B)每克烷類燃燒釋出熱量的大小順序為:甲烷>乙烷>丁烷>戊烷(○)
(C)每克烷類燃燒釋出熱量皆大於50千焦耳(✖)
<修正>由表3換算每克燃燒熱可見有些小於 50 kJ/g。
(D)燃燒2莫耳甲烷燃燒1莫耳乙烷,所釋出的熱量更多(✖)
<修正>燃燒熱比較應以表中數值計算;題幹要比「2莫耳甲烷」與「1莫耳乙烷」需直接乘莫耳燃燒熱後判斷。
(E)…己烷的莫耳燃燒熱約為6200…(✖)
<修正>由表3趨勢,己烷燃燒熱應介於戊烷與辛烷之間,不會高到 6200。
-
第56題,答案:(a) C3H8 (b) 2217 kJ/mol
(a)…丙烷的分子式為何?並計算其分子量為何?
<修正>丙烷分子式:C3H8;分子量:3×12 + 8×1 = 44。
(b)…預測丙烷的莫耳燃燒熱的數值為何?
<修正>以乙烷與丁烷線性估算取平均:(1560 + 2874)/2 = 2217 kJ/mol。
-
第57題,答案:A、C、D
…下列敘述何者正確?(應選2項)
(A)…平衡反應式(○)
(B)…一半來自丙烷,另一半來自丁烷(✖)
<修正>「各占一半」需看質量/莫耳數/燃燒熱,不會必然各半。
(C)…所需氧氣的莫耳數相同(○)
(D)…會產生不同莫耳數的水(○)
(E)…液化天然氣產生較少的二氧化碳(✖)
<修正>需依燃料種類與反應係數計算,不能直接推出「必較少」。
